کاتالیزور ها قهرمانان گمنام واکنش های شیمیایی هستند. این مواد به تسریع واکنشهای شیمیایی کمک میکنند تا به طور موثر پیش بروند.
کاتالیزور چیست؟
کاتالیزور ماده ای است که واکنش های شیمیایی را سرعت می بخشد، اما در واکنش مصرف نمی شود. از این رو یک کاتالیزور را می توان در پایان واکنشی که برای تسریع یا کاتالیز استفاده شده است. بدون تغییر شیمیایی بازیابی کرد .
کارخانه ها برای همه چیز از پلاستیک تا دارو به کاتالیزورها متکی هستند. کاتالیزورها به پردازش نفت و زغال سنگ به سوخت مایع کمک می کنند. آنها بازیگران کلیدی فناوری های انرژی پاک هستند. کاتالیزورهای طبیعی در بدن معروف به آنزیم ها نقش مهمی در هضم و غیره دارند.
در طول هر واکنش شیمیایی، مولکولها پیوندهای شیمیایی بین اتم های خود را میشکنند . اتم ها همچنین پیوندهای جدیدی با اتم های مختلف ایجاد می کنند. این مانند تعویض شریک در یک رقص مربع است.
حالت گذار در کاتالیزور و واکنش های شیمیایی
برای واکنش مواد شیمیایی، پیوندهای آنها باید دوباره مرتب شوند، زیرا پیوندهای موجود در محصولات با پیوندهای موجود در واکنش دهنده ها متفاوت است. کندترین مرحله در بازآرایی پیوند حالت گذار نامیده می شود. یک گونه شیمیایی که نه یک واکنش دهنده است و نه یک محصول، بلکه واسطه بین این دو است.
انرژی فعال سازی را می توان به عنوان مانعی در برابر یک واکنش شیمیایی در نظر گرفت، مانعی که باید از آن عبور کرد. اگر سد زیاد باشد، تعداد کمی از مولکولها انرژی جنبشی کافی برای برخورد، تشکیل یک حالت گذار و عبور از سد را دارند. واکنش دهنده هایی با انرژی کمتر نمی توانند از حالت گذار عبور کرده و واکنش دهند و تبدیل به محصول شوند.
کاتالیزورها سد انرژی را کاهش می دهند. مسیر متفاوت اجازه می دهد تا بازآرایی پیوند مورد نیاز برای تبدیل واکنش دهنده ها به محصولات آسان تر و با ورودی انرژی کمتر انجام شود. در هر بازه زمانی معین، وجود یک کاتالیزور به نسبت بیشتری از گونه های واکنش دهنده اجازه می دهد تا انرژی کافی برای عبور از حالت گذار و تبدیل شدن به محصول را دریافت کنند.
آنزیم ها به عنوان یک کاتالیزور در بدن
در بدن ما و سایر موجودات زنده، از آنزیم ها برای تسریع واکنش های بیوشیمیایی استفاده می شود. آنزیم نوعی کاتالیزور است. بدون وجود آنزیم ها غیر ممکن است که واکنش های شیمیایی با سرعت مناسب و به درستی انجام شوند. شکل آنزیمها همراه با مکانهایی روی آنزیم که به واکنش دهنده ها متصل میشوند. یک مسیر واکنش جایگزین را فراهم میکنند. که به مولکولهای خاص اجازه میدهد تا با هم جمع شوند و یک حالت گذار با سد انرژی فعال سازی کاهش یافته را تشکیل دهند.
در شکل شماتیک زیر، آنزیم با زنجیره بلند، مکان هایی را برای مولکول های واکنش دهنده فراهم می کند تا به هم بپیوندند تا یک حالت گذار با انرژی فعال سازی کم را تشکیل دهند.
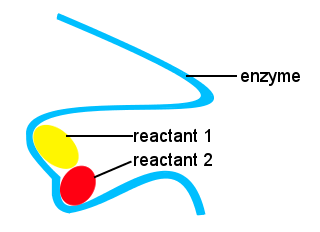
کاتالیزورها نمی توانند موقعیت یک تعادل شیمیایی را تغییر دهند. واکنش های رو به جلو و عقب هر دو شتاب می گیرند به طوری که ثابت تعادل K eq بدون تغییر است. با این حال، با حذف محصولات از مخلوط واکنش به عنوان آنها، سرعت کلی تشکیل محصول را می توان در عمل افزایش داد.
انتقادات و پیشنهادات کاربران گرامی
برای مطالعه سایر مقالات علمی و پزشکی به بخش مقالات وبسایت مستر آزما مراجعه نمایید. در صورت نیاز به مطالعه مقاله ای خاص به کارشناسان ما اطلاع دهید تا مقاله را برای شما روی سایت قرار دهند.نظرات خود را با ما به اشتراک بگذارید.

